Einleitung
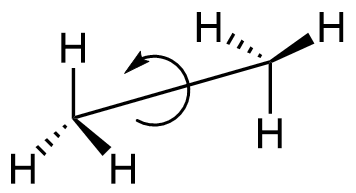
Die Konformation eines Moleküls beschreibt die
räumliche Anordnung der Atome an den drehbaren
Kohlenstoff-Kohlenstoff-Einfachbindungen.
 Weitere Begriffe der Stereochemie lassen sich unter dem Glossareintrag
Isomerie nachschlagen.
Weitere Begriffe der Stereochemie lassen sich unter dem Glossareintrag
Isomerie nachschlagen.
Moleküle, welche die gleiche Konfiguration besitzen, sich jedoch durch Drehung um eine Kohlenstoff-Kohlenstoff-Einfachbindung ineinander überführen lassen, nennt man Konformationen. Siehe dazu auch das Lernmodul zu Ethan: scheLM 3D JS oder scheLM 3D JAVA
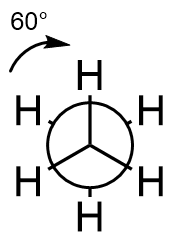 Bei der gestaffelten Konformation eines Moleküls sind die
Subtituenten der beiden Kohlenstoffatome, welche an der
Kohlenstoff-Kohlenstoff-Einfachbindung beteiligt sind, um 60°
zueinander verdreht. Die Substituenten sthen auf Lücke.
Diese Konformation ist energetisch am
günstigsten und stellt ein Energieminimum dar, da die Substituenten
weiter voneinander entfernt sind als zum Beispiel bei der
ekliptischen Konformation.
Bei der gestaffelten Konformation eines Moleküls sind die
Subtituenten der beiden Kohlenstoffatome, welche an der
Kohlenstoff-Kohlenstoff-Einfachbindung beteiligt sind, um 60°
zueinander verdreht. Die Substituenten sthen auf Lücke.
Diese Konformation ist energetisch am
günstigsten und stellt ein Energieminimum dar, da die Substituenten
weiter voneinander entfernt sind als zum Beispiel bei der
ekliptischen Konformation.
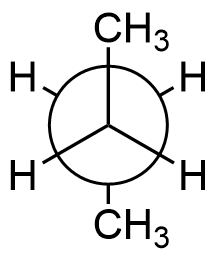
 Betrachtet man die Kohlenstoff-Kohlenstoff-Einfachbindung zwischen dem
zweiten und dritten Kohlenstoffatom im Butanmolekül, erhält man ein
ähnliches Bild wie im oben gezeigten Ethanmolekül.
Als Substituenten sind es hier jedoch nicht drei Wasserstoffatome, sondern zwei
Wasserstoffatome und eine CH3-Gruppe.
Die CH3-Gruppe verfügt über
eine größere Elektronenhülle als die Wasserstoffatome und führt dazu,
dass zwei energetisch unterschiedliche gestaffelte Konformationen
vorhanden sind.
Betrachtet man die Kohlenstoff-Kohlenstoff-Einfachbindung zwischen dem
zweiten und dritten Kohlenstoffatom im Butanmolekül, erhält man ein
ähnliches Bild wie im oben gezeigten Ethanmolekül.
Als Substituenten sind es hier jedoch nicht drei Wasserstoffatome, sondern zwei
Wasserstoffatome und eine CH3-Gruppe.
Die CH3-Gruppe verfügt über
eine größere Elektronenhülle als die Wasserstoffatome und führt dazu,
dass zwei energetisch unterschiedliche gestaffelte Konformationen
vorhanden sind.